
|
分子という分子は何百、何千という多くの原子からできているものをいう。
次に原子の構造を水素(H)、ヘリウム(He)及びリチウム(Li)の原子について述べる。
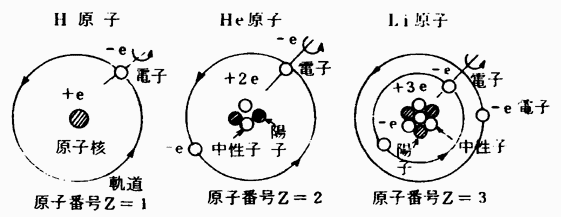
図1・5 原子の構造例
図1・5に示すように、一般に原子の中心には正電荷+Z・e〔C〕をもった1個の原子核と、その周囲を一定の軌道を抽きながら回転している負電荷-e〔C〕をもったZ個の電子(electron)からできている。この場合電子の回転による遠心力と原子核の吸引力とは釣り合っている。
そして原子核の正電荷+eと電子の負電荷-eとは異種であるが等量であるから、原子は全体として中性である。
原子核にあるいくつかの正電荷をもった陽子と電荷をまったくもたないいくつかの中性子は核力によって堅く結ばれていて、原子核から陽子を取り出すことは極めて困難である。この力の場に1935年湯川秀樹博士が中間子という粒子が存在ずることを理論的に説明したことはよく知られている事柄である。こられの電子、隔子、中性子のほか中間子の粒子を総称して素粒子と呼んでいる。
1・4・2束縛電子、自由電子、イオン
(1)束縛電子 束縛電子1・4・1で述べたように、原子核の周囲を力の釣り合いを保って電子が軌道上を回転している状態の電子すなわち束縛された電子をいっている。
(2)自由電子 自由電子は上記とは少し趣きを異にし、外側の電子は運動エネルギーは大きいが原子核からの結びつきは比較的弱いので、したがって、金属元素等で外部からの電気力が働けば軌道からはなれて飛び出す電子ができる。これを自由電子という。例えば、真空管のフィラメントに熱を加えれば自由電子が飛び出すなどはその例である。
(3)イオン 原子において何かの理由で負電子を失えばその分だけ正電荷が多くな
前ページ 目次へ 次ページ
|

|